Biologie Moléculaire et Cellulaire
LES VIRUS - Structure et organisation
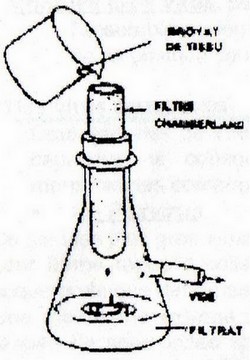
Le filtre Chamberland : découverte des virus
C'est grâce au filtre Chamberland qu'on va suspecter l'existence d'agents infectieux particuliers.
Dès 1881, Pasteur a montré que l'agent infectieux responsable de la rage est invisible au
microscope et qu'il est impossible de l'isoler sur des milieux de culture artificiels. Pasteur
"cultive" l'agent infectieux en partant d'un broyât de cerveau de chien enragé qu'il inocule à la
surface du cerveau d'un lapin trépané.

En 1892, Ivanovski découvre qu'une maladie du tabac (la mosaïque du tabac) peut être
transmise par la sève d'un plant malade passée sur filtre Chamberland et inoculée à une plante saine. Pour lui, l'effet est imputable à
une toxine.
Plus tenace, Bejerinck poursuit l'expérimentation : en inoculant un troisième
plant à partir du second et ainsi de suite, il démontre que l'agent causal n'est pas une
toxine mais un nouveau type d'agent infectieux se multipliant dans les cellules de
son hôte. C'est un "contagium virum fluïdum" : un agent ultrafiltrable (1898).
Dès lors, quand ils parviennent pas à isoler l’agent responsable d’une maladie présumée
infectieuse, les microbiologistes triturent les lésions engendrées au cours de la maladie
infectieuse (végétale ou animale) et filtrent la suspension obtenue sur filtre Chamberland :
Si l’injection du filtrat à une plante ou à un animal sain (de la mpeme espèce que la plante
ou l’animal malade) reproduit la maladie, un virus en est à l’origine.
Rapidement, l’étiologie virale est ainsi démontrée pour de nombreuses maladies.
Ainsi, toute cellule vivante peut être la cible de virus spécifiques et il est possible de distinguer
3 classes de virus, dont les propriétés sont globalement identiques :
virus des végétaux, virus des animaux, virus des bactéries.
Les virus sont de petites particules biologiques de 20 à 300 nm de diamètre dont la structure
résulte de l'assemblage de deux ou trois éléments : le génome, une capside. et parfois une
enveloppe.
Le terme "virus" concerne l'agent infectieux à tous les stades du cycle viral, extracellulaire
ou intracellulaire. Le terme "virion" définit la particule virale infectieuse complète. Il est
constitué :
Cette règle générale a des exceptions : les Poxvirus (virus de la variole) et les Hepadnavirus (Hépatite B) sont des virus enveloppés mais résistants.
1. Capside et enveloppe
La capside
Toutes les nucléocapsides virales (ou presque) sont construites selon deux modèles :
• les virus en bâtonnets ont des nucléocapsides a symétrie hélicoïdale,
• les virus sphériques ont des nucléocapsides à symétrie icosaédrale.
Quelques virus, les gros virus et certains bactériophages, ont des morphologies plus
complexes.
Composition de la capside
L'information génétique des virus étant limitée, la variété et la taille des protéines virales le sont
également.
La structure de protection du génome, la capside, est de nature protéique. Ce ne peut pas être
une protéine géante (qui "consommerait" presque toute l'information génétique), mais un
assemblage de sous-unités protéiques dont la diversité ne peut être que très limitée. On
observe en effet 1 seul type de sous-unité chez les petits virus et une dizaine chez les plus
gros.
Construction de la capside :
La stratégie universelle pour "emballer" l'acide nucléique viral consiste à utiliser un grand
nombre de copies d'une ou plusieurs petites protéines qui vont s'assembler autour du génome.
La capside se forme le plus souvent par un processus d'auto-assemblage. Les éléments
assemblés sont retenus dans leurs positions par des forces d'attraction moléculaire.
L'auto-assemblage implique un arrangement symétrique : c'est à cause de leur symétrie que
certains virus peuvent cristalliser.
Selon la symétrie engendrée par l'agencement des protéines de capside autour de l'acide
nucléique, on distingue 4 types principaux de virus :
- a) les virus à symétrie hélicoïdale :
Chaque sous-unité a une forme particulière qui ménage une rigole au sein de laquelle l'acide nucléique va pouvoir se loger.
Au centre des disques se trouve un site de reconnaissance d'un segment particulier de l'ARN génomique qui permet l'initiation de l'auto-assemblage de la capside.
La nucléocapside forme un cylindre creux dont le diamètre est caractéristique du virus étudié.
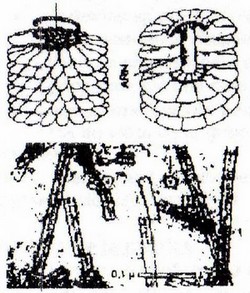
- La nucléocapside peut être une hélice rigide : exclusivement chez des virus végétaux comme le VMT (virus de la mosaïque du tabac).
- La nucléocapside peut être une hélice flexible : c'est le cas de tous les virus animaux à symétrie hélicoïdale (qui sont tous, par ailleurs, des virus à ARN enveloppés).
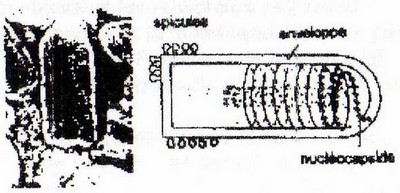
La morphologie du virus de la rage est caractéristique : la nucléocapside est embobinée dans une enveloppe qui donne au virion l’apparence d’un obus (ou d’un supposotoire…).
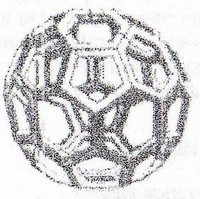
- b) Les virus à symétrie icosaédrale :
Une observation plus fine révèle que ces capsides, quasiment sphériques, sont des icosaèdres. L'icosaèdre est un polyèdre obtenu par l'assemblage de 20 triangles équilatéraux (icosa = 20) :
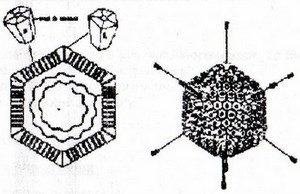
chez les petits virus : comme le virus poliomyélitique, il ne semble pas y avoir d'autres
protéines de structure que celle de la capside.
chez les gros virus : par contre, le génome peut être associé à une ou plusieurs protéines :
l'ensemble génome + protèine(s) forme un nucléoïde (ou "core" pour les anglais, en raison de
sa position centrale).
- c) Les virus complexes :
·Les Poxvirus
Ce sont les plus gros virus connus (on peut déjà les apercevoir au microscope photonique). Leur forme rappelle celle d'un petit bacille. En coupe, un nucléoïde central semble entouré d'une coque protéique déprimée au centre par deux corps latéraux.
Une membrane externe apparaît comme recouverte d'une série de tubes composés d'une double rangée de sous-unités sphériques réparties au hasard (virus de la variole) ou sous la forme d'un filament continu encerclant la particule (virus Orf du mouton).

·Les phages caudés (cf . cours sur les phages)
- d) Les virus à symétrie non déterminée : les lentivirus
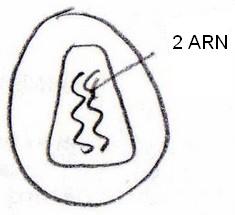
Cette sous-famille des rétrovirus comprend notamment les virus du sida (virus de l'immunodéficience humaine ou VIH). Leur capside prend un aspect en "tronc de cône", caractéristique mais qui reste à définir complètement.
Fonctions de la capside
- a) Fonction de protection
- b) Fonction de fixation
L'enveloppe
La présence d'une enveloppe caractérise les virus enveloppés.
La nucléocapside est entourée d'une enveloppe, encore appelée peplos (= le manteau) : c'est
donc l'élément le plus externe du virion.
L'enveloppe dérive d'une membrane de la cellule-hôte !
« L’enveloppe » ou « peplos » évoquent une structure souple et, de fait, l'enveloppe est acquise
lorsque les nucléocapsides traversent l'une des membranes de la cellule-hôte :
- ·la membrane cytoplasmique (cas le plus fréquent) : par exemple, le virus de la rougeole
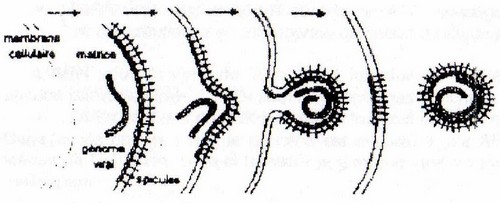
- ·la membrane nucléaire : les virus de l'herpès
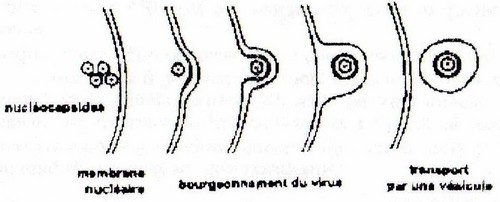
- ·une membrane du réticulum endoplasmique : les flavivirus (virus de la fièvre jaune).
En fait, l'enveloppe est un fragment de membrane cellulaire complètement remanié : la cellule ne fournil que la double couche lipidique. Les protéines et glycoprotéines cellulaires sont déplacées et remplacées par des protéines et des glycoprotéines virales.
- a) Les spicules glycoprotéiques
Les glycoprotéines s'insèrent dans la membrane lipidique par une région hydrophobe de leur chaîne polypeptidique. L'extrémité est en contact avec la nucléocapside ou avec la matrice sous-jacente. Les glyocoprotéines sont habituellement associées en oligomères (di, tri ou tétramères) plus ou moins visibles au microscope électronique sous la forme de spicules (encore appelées peplomères).
Fonctions des spicules
· les spicules portent les déterminants qui reconnaissent les récepteurs cellulaires.
· certaines spicules favorisent la fusion de l'enveloppe avec la membrane cellulaire par l'action d'une séquence d'acides aminés hydrophobes (la protéine F du virus de la rougeole).
· d'autres spicules peuvent exercer des activités enzymatiques (la protéine NA du virus de la grippe qui est une neuraminidase).
· une même spicule peut exercer successivement la reconnaissance et la fusion (les protéine HA du virus de la grippe ; les spicules des virus de l'immunodéficience humaine).
- b) La matrice
Fonctions de la matrice
· la matrice renforce la double couche lipidique et stabilise la nucléocapside.
· par ses relations avec les spicules et avec la nucléocapside, la matrice intervient dans l'assemblage des futures particules virales.
2. Génome des virus
Le génome des virus est constituée d'ADN ou d'ARN. Celle propriété permet de classer les
virus en deux groupes :
- les virus a ADN
- les virus à ARN
La structure du génome
La structure du génome est extrêmement variable.
Si les virus ont pour origine une information génétique cellulaire qui a pris son indépendance,
on doit s'attendre à pouvoir retrouver une certaine parente dans la structure des génomes :
dans la cellule, l'ADN se trouve sous forme bicaténaire et l'ARN sous forme monocaténaire. En
ce qui concerne les virus animaux, on a décrit les structures suivantes :
Malgré les apparences, ce sont les virus à ARN qui présentent une variété considérable de structures.
La taille du génome
L'information génétique est proportionnelle à la taille du virus.
D'après la taille du génome en kb (1kb, 300 codons, 1 protéine) on peut estimer le nombre de protéines virales (de 3 à 300).
Mais certains virus augmentent leurs capacités de codage car ils ont des gènes chevauchants: un même segment, lu dans des cadres de lecture différents, peut être traduit en 2 ou 3 protéines.
L'originalité des virus à ARN
a) Première originalité : un génome modeste
• le génome des virus à ADN varie de 3 à 280 kb,• le génome des virus à ARN ne s'écarte pas d'une taille moyenne de 15 kb.
-> parce qu'un ARN monocaténaire est fragile
La taille d'un génome ARN ne doit pas dépasser une certaine limite au-delà de laquelle les risques de cassure sont importants.
Une cassure entraîne l'inactivation du virion.
Certains virus à ARN ont contourné la difficulté en segmentant leur génome. Ils doivent toutefois résoudre un problème nouveau: le réassortiment exact, car chaque virion doit posséder un exemplaire de chacun des segments, sous peine d'être inactivé.
-> parce que les ARN-polymérases sont imprécises
Les virus à ADN vont utiliser l'ADN polymérase de la cellule :
• or l'ADN polymérase dispose d'une fonction de relecture : si le nucléotide qui vient d'être incorporé est incorrect, il est immédiatement éliminé par l'enzyme.
• la cellule est en outre dotée de nombreux systèmes de réparation de l'ADN dont les virus profitent : les erreurs qui surviennent au cours de leur réplication peuvent ètie corrigées.
Les taux de mutation sont donc extrêmement faibles : de 1/108 à 1/109 , soit 1 nucléotide erroné pour 10 millions à 1 milliard de nucléotides recopiés.
Les virus à ARN ne peuvent utiliser l'ARN polymérase cellulaire :
• les ARN polymérases cellulaires sont exclusivement ADN dépendantes, elles ne peuvent transcrire que de l'ADN : le virus doit donc être capable de fabriquer une transcriptase ARN dépendante.
• comme les ARN polymérases cellulaires, les ARN polymérases, virales n'ont pas de fonction de relecture.
• la cellule ne possède pas de système de réparation de l'ARN Les taux de mutation sont très élevés : en moyenne de 1/103 à 1/104 soit 1 nucléotide erroné pour 1000 à 10.000 nucléotides recopiés.
A ces taux, un génome de 100 kb (105 bases) comporterait 10 à 100 mutations, et vraisemblablement la plupart de ces mutations seraient létales : les virions obtenus ne seraient pas viables.
Le génome des virus à ARN est donc condamné à rester modeste !
Un taux de mutation élevé représente toutefois un avantage pour les virus à ARN : l'apparition fréquente de mutants qui échappent au système immunitaire de l'hôte, (cf. les virus de la grippe et les virus du sida).
b) Deuxième originalité : des virus à ARN + et des virus à ARN –
L'ARN seul du virus poliomyélitique est introduit dans une cellule sensible : celle-ci fabrique des
particules virales complètes comme si elle avait été infectée par le virion. (ARN +)
• l'ARN viral s'est comporté comme un ARN messager. les ribosomes ont pu s'assembler sur
un site d'initiation et ont reconnu un codon d'initiation AUG.
L'ARN seul du virus de la rage est introduit dans une cellule sensible : la cellule ne fabrique
aucune particule virale. L'ARN seul n'est donc pas infectieux. (ARN -)
• l'ARN viral doit donc être d'abord transcrit en ARN messager.
Dans le cas de ces virus, le génome est associé à une ARN polymérase virale. Dans les
piemiers stades de l'infection, celle-ci transcrit le génome viral en plusieurs ARN "positifs" : ce
sont les ARN-messagers.
c) Troisième originalité : la segmentation du génome
Certains virus à ARN ont un génome composé de plusieurs segments, les virus de la grippe par
exemple.
La segmentation d'un génome viral a une conséquence remarquable :
Deux virus à génome segmenté appartenant à la même espèce, (le virus de la grippe A, par
exemple) mais génétiquement différents peuvent infecter simultanément une même cellule et
s'y multiplier. Au moment de l'assemblage des virions, le réassortiment des segments
génétiques peut donner naissance à un virus nouveau (qui, dans l'exemple d'un virus grippal
pourra être à l'origine d'une épidémie mondiale, une pandémie).
Quelques arbovirus (Arenavims et Bunyavims) ont un génome ARN segmenté tout à fait
particulier puisque certains segments sont ambivalents : une partie majeure ARN - est soudée à
une partie mineure ARN. Une transcriptase est associée à la nucleocapside.
Une famille de virus animaux, les Reovirus, ont un génome constitué par 10 segments d'ARN
bicaténaire. Une transcriptase est associée à la nucleocapside afin d'assurer la transcription en
ARN messager de chaque segment.