Microbiologie
Le Pouvoir Invasif
Le pouvoir invasif repose sur deux grands facteurs liés à la bactérie:
– la production de toxines
– et la capacité à envahir l'hôte.
C'est cette capacité à envahir que l'on appelle « pouvoir invasif ». Celui-ci s'appuie sur
toutes les structures de la bactéries qui va lui permettre de rester dans l'hôte et de s'y multiplier.
1. Infection localisée
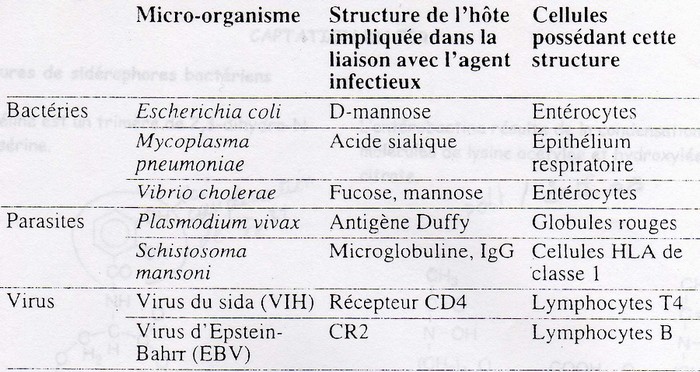
Adhérence et adhésion
Adhérence: phénomène non spécifique, due aux attractions électrostatiques.
Adhésion: phénomène spécifique; phénomène de reconnaissance moléculaire entre une
adésine coté bactérie et de son récepteur coté cellule.
L'action de fixation est un phénomène essentiel dans le pouvoir invasif.
Par ex: enfants avec gastro. = ici E. coli 80% de facteurs d'adhésion aux entérocytes
enfants sans gastro. = E. coli 17% de facteurs d'adhésion.
Si on inhibe la fixation (cad l'adhésion) avec des molécules leurres qui vont se fixer au
niveau des adésines bactériennes, on peut bloquer le processus infectieux.
Mais le seul fait de se fixer n'est pas pathogène. En effet la fixation donne la résistance vis
à vis des contraintes mécaniques (comme la toux, flux urinaires, tout ce qui vise à évacuer
les intrus). La fixation bactérienne sert de point d'encrage à la bactérie pour se coloniser,
mais sert aussi à la production locale de toxines.
L'adhérence est notamment vu sur les surfaces inertes comme par ex. les biofilms, d'où le
choix judicieux des matériaux médicaux.
L'adhésion aux niveau des cellules est due à des structures aux surfaces des cellules,
notamment des structures glycosilées.
Structure de reconnaissance = site où la bactérie peut se fixer pour envahir, se sont des
glycoprotéines situées dans le matrice extracellulaire comme la fibronectine.
L'invasion
C'est la capacité d'un organisme à pénétrer dans les tissus avec d'abord l'invasion par les
cellules épithéliales. Cela permet d'éviter tous les mécanismes de défenses extracellulaires
(comme les Ac). Cela favorise également la colonisation. Permet aux microorganismes
d'accéder à un milieu riche comme le cytoplasme.
L'invasion de fait par deux étapes:
– internalisation:
« Diacytose » = perforation de la membrane et entrée directe dans le cytoplasme. Très
peu de microbes le font, il s'agit d'un phénomène exceptionnel.
« Phagocytose ».
– dans la cellules:
le microbe ne doit pas rester trop longtemps dans le phagosome car il risque de fusionner
avec le lysozome ce qui entrainerait sa dégradation.
Par ex: Shigella provoque, grâce à l'internalisation de la bactérie, une reconnaissance de la
cellule épithéliale, ce qui entraine la formation d'une liaison bactérie – cellule. Il y a alors
un réarrangement du cytosquelette pour entrainer la phagocytose de la bactérie. Il y a
donc création d'un phagosome qui s'acidifie ce qui active une enzyme : la « listériolysine »
responsable de la lyse du phagosome. La bactérie est alors libérée dans le cytoplasme, elle
est alors capable d'envahir tout un épithélium.
Shigella et Listeria ont le même mécanisme d'invasion.
Mycobacterium fera en sorte que l'environnement du phagosome ne lui soit pas trop
néfaste, il empêche la fusion avec le lysozome.
Yersinia pestis est capable de résister aux conditions extrêmes du phagosome, même si
cela est très néfaste pour le microbe.
2. Dissémination dans l'organisme
Pour que le germe puisse métastaser, il faut qu'il passe dans la circulation générale afin de se déplacer et atteindre un organe interne où il pourra de nouveau s'implanter et se multiplier.
Les voies de dissémination dans l'hôte
Une fois que les germes ont passé la barrière des muqueuses, la principale voie est celle
des canaux lymphatiques. Pourquoi? Car il s'agit d'un réseau très important notamment au
niveau digestif qui permet de drainer tout l'organisme. Les cellules n'ont pas de cohérence
et sont non-jointives mais juste superposées. Il n'y a aucune barrières physiques alors les germens passent mieux.
Le passage du pathogène au niveau du ganglion peut alors le neutraliser.
De plus la voie lymphatique finie dans la voie sanguine.
Du moment où il y a un pathogène dans le sang = « septicémie », dès lors il peut y avoir accès à n'importe quel organe.
Cependant c'est rarement dans le sang que se fait la croissance bactérienne car c'est un milieu défavorable notamment dans la disponibilité en fer.
Le rôle du fer
Pour une croissance correcte des bactéries il faut une concentration en fer de 10-6 mol/L. Or
la concentration en fer libre de l'organisme est de 10-18 mol/L car le fer est séquestré par la
transferrine (sérum) qui est chargée de le transporter.
On a noté que l'augmentation de la concentration en fer est défavorable pour le système
immunitaire. En effet la diminution de la concentration en fer entraine la diminution du
chimiotactisme, diminue l'effet bactéricide de la phagocytose, entraine des saignements au niveau des muqueuses.
Par ex: le phénomène d'Hypersidérémie dans le sang chez les cobayes. Chute de 6 à 7 log de la DL50 de Yersinia.
Les bactéries vont donc mettre en oeuvre des phénomènes de captation du fer.
La bactéries secrètent des « sidérophores » qui vont être capables de complexer le fer en
Fe3+ avec une constante d'association KA = 1030. En plus des sidérophores, il existe des
récepteurs qui captent les complexes [ sidérophores – Fe3+ ].
3. Le pathogène évite les défenses de l'hôte
Camouflage par la capsule
Lien entre la capsule et le pouvoir pathogène:
Structure très fortement liée à l'expression du pouvoir pathogène.
Il existe 3 mécanismes:
– non-reconnaissance: cad quand il y la capsule, le système immunitaire aura du mal a
reconnaître le microbe, les Ig ne sont alors pas capables de se fixer.
– Inhibition de la phagocytose: la capsule empêche l'optionisation, le complément n'est pas stimuler.
– Phénomène de mimétisme moléculaire: structure proche en polyosides des cellules
Eucaryotes, il y a un leurre dans le système immunitaire.
Ex Strep. pyogènes: structure riche en acide hyaluronique qui ressemble bcp à des molécules de surface des cellules Eucaryotes.
Résistance aux macrophages
Il existe des bactéries capables de résister aux macrophages. Certaines bactéries
empêchent qu'il y ait fusion entre le phagosome et le lysozome.
D'autres survivent dans un compartiment modifié (Yersinia, Legionella). Elles peuvent
résister aux phagosomes grâce à des enzymes. En effet ces enzymes agissent contre le
pouvoir oxydant, donc améliore la « vie » dans le phagosome.
Résistance au système immunitaire spécifique
Variations antigéniques
C'est la capacité du microbe à exprimer successivement dans le temps différents épitopes dans ses composants de surface.
Principe: problème de cinétique du Système Immunitaire. Cad entre le moment où le
microorganisme entre dans l'hôte et le moment où il y a une réponse immunitaire contre le
microorganisme = environ plusieurs jours. Or pendant ce laps de temps il y a apparition de
variants. Donc les Ac produits ne vont détruire que la population qu'ils ont reconnu. Et les
autres variants, mêmes très minoritaires pourront conduire un nouveau cycle infectieux.
Mécanisme très connu chez les virus, notamment pour la grippe.
Destruction spécifique des Ac
Ex: Neisseria gonorrhae, Haemophilus influenzae, Streptococcus pneumoniae
=>ils produisent tous des protéases contre les IgA (Ig au niveau des muqueuses)
Retournement des Ac
Il existe des germes capables de fixer les Ac par fragment Fc (ex: Staph. aureus)
Tolérance immunitaire
C'est l'absence de réponse immunitaire vav du « Soi ». Ceci s'acquiert naturellement au cours du développement, ça entraine des phénomènes de délétions clonales et d'anergie = maturation normale du système immunitaire. Le phénomène existe aussi vav des flores commensales du Tube Digestif ce qui explique qu'il y ait absence de réaction immunitaire pour certains germes commun tu TD comme les bactérioïdes.
4. Annexes.
Documents associés
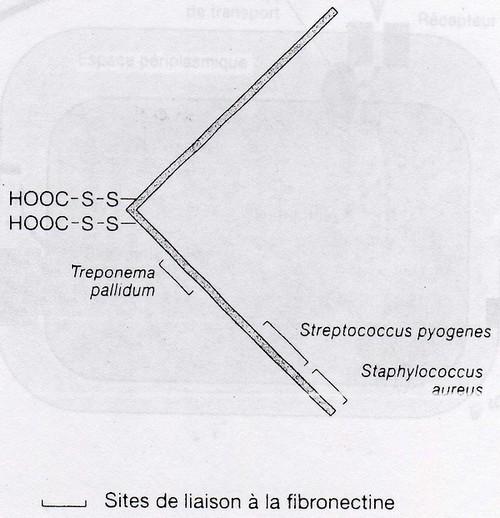
Sidérophores bactériens:
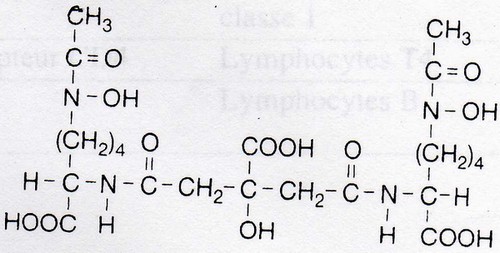
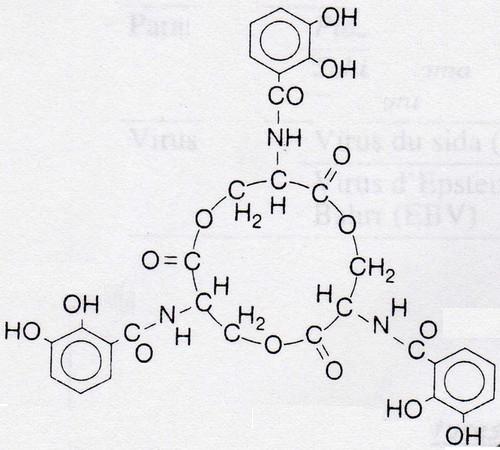
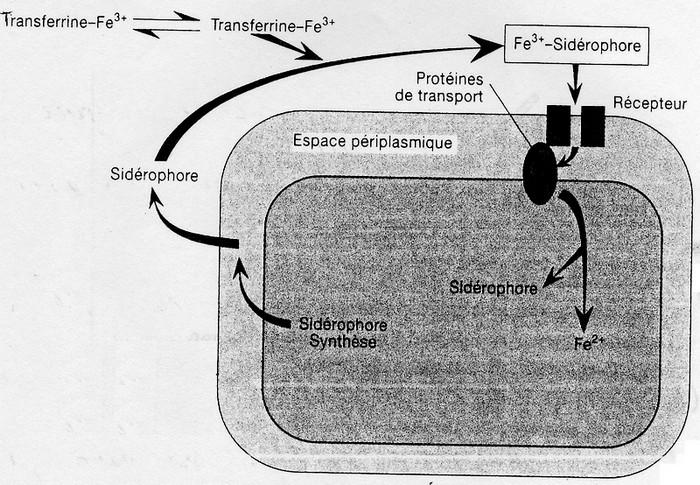
Transfert du Fer chez E. coli: