Biochimie
LES ACIDES NUCLEIQUES
On distingue 2 catégories d'acides nucléiques:
L'ADN: Acide DésoxyriboNucléique
Il est présent:
- chez les Eucaryotes: dans le noyau (chromosomes et chromatine)
dans les mitochondries et chloroplastes
- chez les bactéries: chromosome
plasmides
- chez les virus à ADN: enfermé dans une coque protéique avec éventuellement enveloppe lipidique
Il est, chez les Eucaryotes, associé à des protéines (nucléoprotéines). Il est le support de l'information génétique.
L'ARN: Acide RiboNucléique
Ils sont présents:
- chez les Eucaryotes: dans le noyau (nucléoles, ARNr)
dans le cytoplasme: libres ou associés à des protéines (ribosomes)
dans les mitochondries et chloroplastes
- chez les bactéries: dans le cytoplasme
- chez les virus: idem plus haut
Les ARN permettent l'expression de l'information génétique portée par l'ADN. Chez
certains virus, l'ARN est le support de l'information génétique.
1. Structure Primaire Des Acides Nucléiques
ADN et ARN sont des polynucléotides.
Ils sont formés de l'enchaînement des nucléosides 5' monophosphates via les pentoses, grâce à des liaisons 3'-5'phosphodiesters
fonction alcool en 3' de l'un est estérifiée par une fonction de l'acide phosphorique lié en 5' de l'autre.
Ainsi, l'acide phosphorique engage 2 liaisons acides dans des fonctions phosphodiester; la
3ème fonction acide reste libre et confère donc des propriétés acides aux "acides" nucléiques.
Les bases azotées ne sont pas impliquées dans les liaisons entre monomères.
Il se forme ainsi un enchaînement de nucléotides du type 5'-3-5'-3', conduisant à un dinucléotide, puis à des polynucléotides.
La séquences des nucléotides, donnée par celle des bases, représente la structure primaire des acides nucléiques.
Ainsi, une chaîne polynucléotidique va être caractérisée par:
1- La nature du pentose des nucléotides engagés: ribose (--> ARN), désoxyribose (--> ADN)
2- Le nombre, la nature et la séquence de ces nucléotides: ainsi, comme pour les protéines, on appelle séquence l'ordre dans lequel les
nucléotides sont engagés. L'ADN est donc une combinaison des 4 nucléosides dA, dT, dG, dC et l'ARN de A, U, G, C.
3- La présence d'une extrémité portant un groupement phosphate sur le C 5': c'est l'extrémité 5'phosphate.
4- La présence d'une extrémité portant un groupement OH sur le C 3': c'est l'extrémité 5'OH
5- Conséquences: conventions d'écriture.
La séquence d'un acide nucléique est représentée d'une façon linéaire; se lit de gauche à droite depuis le 5'phosphate au 3'OH. Chaque nucléoside
est désigné par l'abréviation de la base azotée.
Exemple: ADN: 5' (P) A-G-G-T-C-G-C-G-T-(OH) 3'
2. L'ADN: Structures Et Propriétés
Observations
L'ADN a été isolé en 1868 mais son rôle dans le support de l'information génétique n'a été démontré que plus tard (cf plus loin). Des
travaux complémentaires sur sa structure n'ont donc eu lieu que dans les années 1950.
On a constaté un certain nombre de faits:
– dans l'ADN, la quantité d'A = la quantité de T; [C] = [G]. Par conséquent on a l'égalité de concentration entre les bases Puiriques et les bases
pyrimidiques.
– Le rapport des [A+T] / [C+G] est caractéristique d'une espèce. Il est supérieur à 1 chez les animaux et végétaux.
– sous sa forme native, l'ADN présente une viscosité est une densité plus élevée que ne le laisserait supposer une fibre unique,
– à pH physiologique, les fonctions aminés -NH2 et les groupements -CO-NH- sont masqués et ne réagissent que pour 5 < pH < 1 1, ce qui laisse
supposer la présence de liaisons faibles,
– l'ADN natif présente une absorption dans l'UV < l'absorption théorique calculée d'après l'absorption des nucléotides qui le composent
– les études de diffraction aux rayons X suggèrent une forme hélicoïdale.
Modèle de la double hélice (Watson et Crick, 1953)
W et C se sont servis des résultats précédents pour proposer leur modèle:
- La molécule d'ADN est formée de 2 chaînes de polydésoxyribonucléotides enroulées pour former une double hélice. Les bases azotées sont dirigées
dans le centre de l'hélice et les plans formés par les cycles des bases sont parallèles les uns aux autres et perpendiculaires à l'axe de l'hélice.
L'ADN est dit ainsi bicaténaire.
Le pas de l'hélice est de 3,4 nm, avec 10 plans par pas (soit une distance de 0,34 nm entre 2 plans).
L'hélice est droite.
Il existe 2 sillons de taille inégale, le petit et le grand sillon, qui permettent l'accessibilité de l'ADN aux protéines (enzymes de la
réplication et de la transcription,...)
- Les 2 brins sont complémentaires : les bases A et T, ainsi que C et G sont dites complémentaires sont liées entre elles par des liaisons hydrogène
(2 entre A et T, 3 entre C et G).
La connaissance de la séquence de l'un des brins permet de déterminer celle du brin opposé qui lui sera complémentaire.
- Les 2 brins sont antiparallèles, càd qu'ils "vont" dans des directions opposées:
orientation tête-bêche 3'-5' pour l'un et 5'-3' pour l'autre.
La double hélice représente la structure seconde de l'ADN.
Rq: il existe une forme plus rare de l'ADN, dite forme Z, caractérisée par une hélice gauche, il semble que chez les eucaryotcs, certaines régions
sont sous forme Z, mais leur rôle exact est mal connu.
Ainsi, de même qu'une protéine est caractérisée par son nombre d'acides aminés, une molécule d'ADN sera caractérisée par son nombre de nucléotides,
usuellement exprimé en nombre de paires de bases (pb). Par exemple, un ADN de 1000 pb est formé de 2 brins complémentaires de 1000 nucléotides chacun.
A retenir: MM 1 pb = 600 g. mol-1 environ
Configuration bicaténaire hélicoïdale
Représentation de la double hélice d'ADN
a-structure chimique déroulée ("en escabeau") de deux brins complémentaires et antiparallèle appariés;
b-modèle montrant l'enroulement droit des deux brins;
c-modélisation en mode compact d'un fragment de 21 paires de bases.

Liaisons hydrogènes entre les bases
Dans la double hélice, les 2 chaînes sont reliées par des liaisons hydrogène entre bases azotées: 2 liaisons H entre A et T, 3 liaisons H entre
G et C.


Structures d'ordre supérieur: topoisomères et topoisomérases
Topoisomères
- Définition
On appelle alors «topoisomères» ces 2 ADN ne différant que par le nombre d'enlacements.
Les notions qui vont suivre ne s'appliquent théoriquement qu'aux ADN circulaires, c'est-à dire qui n'ont pas d'extrémité libre. Cependant, un ADN linéaire peut se comporter comme un ADN circulaire si chacune de ses deux extrémités est liée à un point d'ancrage, ce qui est en fait le cas dans les cellules.
Le «nombre d'enlacements» est une constante topologique: quelles que soient les déformations que l'on fasse subir à une molécule d'ADN dont les extrémités sont fixes, on ne changera pas le nombre d'enlacements. Un changement de nombre de paire de bases en un endroit d'une boucle d'une molécule d'ADN sera donc obligatoirement compensé par un surenroulement opposé en amont ou en aval de cet endroit.
- Différents états de topoisomères
- Etat surenroulé: l'axe de l'hélice peut s'enrouler sur lui-même en formant une superhélice. Il existe deux possibilités de surenroulement.
> Surenroulement positif: le nombre d'enlacement a augmenté, l'enroulement de la double hélice s'effectue dans le même sens -> super hélice droite.
> Surenroulement négatif: le nombre d'enlacement a diminué, l'axe de l'hélice s'enroule dans le sens opposé à celui de la double hélice, selon une superhélice «négative», gauche --> ceci favorise le déroulement et la séparation locale des deux brins.
Le surenroulement exerce une contrainte sur la molécule: cette contrainte provoque un vrillage aussi bien pour un surenroulement positif que négatif.
L'obtention d'un surenroulement nécessite un apport d'énergie.
La plupart des molécules d'ADN rencontrées dans la nature forment des superhélices gauches. Ce type de molécules est plus accessible aux enzymes de la transcription et de la réplication.
On peut séparer des topoisomères sur gel: plus un anneau d'ADN est désenroulé (= superenroulé négativement), plus il est vrillé, donc plus il est compact: théoriquement, il migrera plus qu'un ADN sous forme linéaire. Cependant, ce n'est pas toujours le cas, car la migration dépend de nombreux autres facteurs.
Topoisomérases
- Définition
- Les différentes topoisomérases
Les topoisomérases I: elles ne coupent qu'un brin de l'ADN bicaténaire. La coupure d'un des brins se fait au niveau d'une liaison phosphodiester, l'extrémité 3'OH reste libre tandis que le phosphate en 5' estérifie momentanément une tyrosine de l'enzyme. Le brin coupé peut alors tourner librement autour du brin intact, puis la liaison phosphodiester est rétablie.
Ces topoisomérases permettent de relâcher des superhélices sous tension. Elles existent chez les Procaryotes et les Eucaryotes.
Les topoisomérases II: Elles coupent les 2 brins de l'ADN bicaténaire. Elles sont dimériques, chaque brin étant coupé par une sous-unité.
- Intérêt des topoisomérases
• L'ADN vrillé est plus compact, donc est plus facile à empaqueter dans un petit volume.
• Les topoisomérases facilitent le réplication, la transcription et la réparation de l'ADN: l'ARN polymérase ne se liera à l'ADN que s'il est désenroulé.
- Eucaryotes:
• En plus des deux intérêts ci-dessus, les topoisomérases peuvent démêler les noeuds d'ADN.
- Application médicale des topoisomérases
Les inhibiteurs des topoisomérases humaines sont des anticancéreux.


Diversité de l'ADN dans le monde vivant
La quantité d'ADN dans les cellules vivantes est très variable d'une espèce à l'autre. Bien avoir en tête l'ordre de grandeur de la taille moyenne d'un génome:
- viral 10^4 à 10^5 pb
- bactérien 10^6 pb
- humain 10^9 pb
Chez les Eucaryotes
L'ADN est contenu dans le noyau de la cellule. Il y a plusieurs molécules d'ADN par cellule. Il est organisé en double hélice
linéaire, selon le modèle de W et C. L'ADN total, chez un homme, s'il était déroulé, représenterait une longueur de 2,30m: il est donc
compacté, grâce à un système de protéines, les histones et les protamines (protéines basiques) ainsi que d'autres protéines non basiques.
On distingue 2 types d'organisation (cf cours de BCM):
- chromatine (cellules en interphase): fibre de 30 nm de diamètre, que l'on peut dérouler artificiellement par traitement chimique; on obtient alors
la structure dite "en collier de perles". Chaque perle est un nucléosome = noyau protéique (8 histones) + enroulement de 146 pb d'ADN autour de ce
noyau. Entre les perles, on a de l'ADN nu (ou presque).
- chromosomes (cellules en division), ils représentent le degré maximal de compaction (longueur 8000 fois plus petite que l'ADN qu'il contient).
Le nombre de chromosomes dans le noyau est caractéristique de chaque espèce.
Il existe un ADN particulier dans les mitochondries (et dans les chloroplastes):
- composé de 2 brins
- circulaire
- il code des ARNr, t, et m.
- le code génétique mitochondriale et légèrement différent du code nucléaire.
- l'hérédité de l'ADN mitochodrial est cytoplasmique: seul l'ADN mitochondriale de la mère est transmis (car le spermatozoïde ne transmet pas de mitochondrie).
Chez les Procaryotes
On trouve chez les bactéries 2 types d'ADN:
- ADN chromosomique: Il y a une seule molécule d'ADN par cellule.
C'est un ADN circulaire d'environ 1Mpb. Il existe également des protéines assurant une certaine compaction (on a longtemps cru qu'il n'y en avait pas).
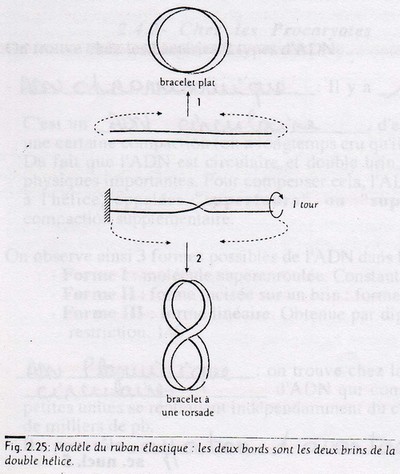
Du fait que l'ADN est circulaire et double brin, la forme en hélice cause une torsion et des contraintes physiques importantes. Pour compenser cela,
l'ADN réalise des boucles tournant en sens inverse par rapport à l'hélice, appelées "supertours" ou "superenroulements". Cela permet en plus un
degré de compaction supplémentaire.
On observe ainsi 3 formes possibles de l'ADN dans la cellule:
- Forme I: molécule superenroulée. Constante de sédimentation: 20S
- Forme II: forme incisée sur un brin: forme intermédiaire isolée dans les préparations d'ADN, 16S
- Forme III: forme linéaire. Obtenue par digestion de l'ADN par les DNases ou les endonucléases de restriction. 14S
- ADN plasmidique: on trouve chez la plupart des bactéries des petites molécules circulaires d'ADN qui constituent l'ADN extrachromosnique ou
plasmides. Ces petites unités se répliquent indépendamment du chromosome. Elles renferment quelques milliers à dizaines de milliers de pb.
Il a pour rôle d'apporter un avantage sélectif aux bactéries qui le possèdent.
Ils sont souvent transmissibles entre bactéries (--> l'apparition de souches résistantes aux antibiotiques dans les hôpitaux). En outre, ces
plasmides sont des outils essentiels au génie génétique (voir plus tard).
Chez les Virus à ADN
Les virus sont des particules formées de l'association d'un seul acide nucléique et des protéines, constituant la nucléocapside.
Certains virus ont en plus une enveloppe lipidique (cf Microbio). Ils possèdent les acides nucléiques les plus courts... et parfois
simple brin.
Le virus a dans son ADN les gènes codant pour ses protéines de capside ou d'enveloppe, ainsi que pour des enzymes particuliers. Il est donc
parasite obligatoire et va détourner le métabolisme cellulaire à son profit (pour cette incapacité à se reproduire seul et pour cette
absence de métabolisme, les virus ne sont pas considérés par les biologistes comme des êtres vivants).
Propriétés de l'ADN
Elles sont dues d'une part à sa composition (nucléotides) et à sa structure (longues chaînes, double hélice).
Absorption dans l'UV
Nous avons vu dans le 1er chapitre que les bases azotées; du fait de leur structure aromatique, absorbent fortement dans l'UV, avec
un maximum à 260nm.
On peut ainsi, à condition de posséder un spectrophotomètre ayant une lampe UV et d'opérer dans des cuves spéciales (cuves en quartz, mais
maintenant cuves en polystyrène plus économiques...), doser l'ADN par mesure de l'absorbance à 260 nm.
Nécessité technique: la solution d'ADN doit être pure. En effet, dans les protocoles de purification de l'ADN, on peut contaminer la préparation
d'ADN par des protéines (qui absorbent elles aussi fortement dans l'UV): on mesure alors le rapport A260/A280 nm.
Rq: L'ADN simple brin absorbe plus que l'ADN double brin: cela vient du fait que dans l'ADN double brin, les bases sont partiellement masquées.
Effet de la température: notions de dénaturation et de renaturation
- Dénaturation
*Conséquences: Comme l'ADN dénaturé est simple brin,
- la viscosité diminue;
- l'absorbance augmente: c'est l'effet hyperchrome.
On peut suivre l'absorbance en fonction de la température; on obtient la courbe de dénaturation. Celle-ci a une allure sigmoïde. Elle possède un point d'inflexion qui correspond à la température à laquelle des molécules d'ADN est dénaturée. Cette température particulière est le Tm ou point de fusion (m pour "melting").
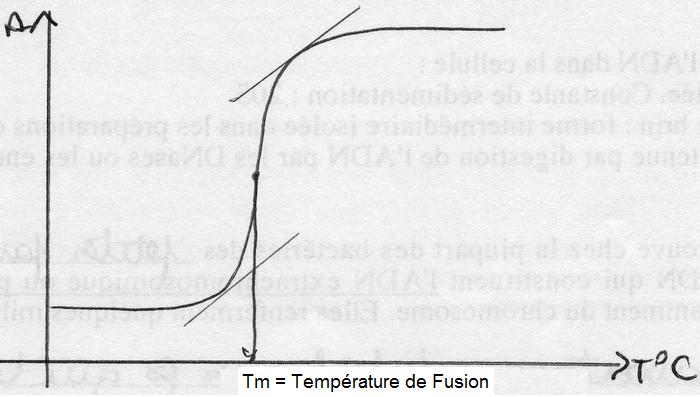
*Facteurs de variation du Tm d'un ADN:
- le Tm dépend du pH et de la force ionique. En effet, la double hélice est d'autant plus stable que les forces de répulsion entre groupements phosphates de chaque brin vont être faibles.
- mais surtout, le Tm dépend de la composition en bases de l'ADN. On a vu que la température rompt les liaisons hydrogènes entre chaque brin d'ADN. Or, il y a 2 liaisons à rompre entre chaque A-T et 3 entre chaque G-C; ainsi, le Tm dépend de la teneur de l'ADN en GC: le Tm augmente de 0,4°C lorsque le % de GC augmente de 1%.
*Applications:
- la mesure du Tm permet d'avoir une idée de la composition en bases de l'ADN.
- le % en GC est utilisé comme critère de classification des bactéries. En effet, des espèces d'un même genre bactérien ont des % en GC proches.
- Renaturation
- refroidissement rapide (ex: mettre l'ADN ayant été chauffé dans la glace).
L'ADN reste dénaturé en grande partie.
- refroidissement lent (ex: on laisse le tube sur la paillasse). Les 2 brins complémentaires se réassocient et on retrouve l'ADN db de départ. L'ADN est dit renaturé ou encore rehybridé.
*Application: Le chauffage de l'ADN suivi d'un refroidissement lent est à la base d'une technique importante de biologie moléculaire: l'hybridation. Celle-ci est possible dès que l'on dispose de 2 simple brins complémentaires (ADN/ADN ou ARN/ADN). Cela permet de repérer un fragment d'ADN ou d'ARN connu dans un milieu (sur un gel d'agarose, sur une coupe de tissus,...) en y fixant un fragment de séquence complémentaire, en général radioactif ou fluorescent que l'on appelle alors sonde moléculaire.
Solubilité
- L'ADN est soluble dans l'eau et les solutions salines à faible concentration.
- En concentration saline plus importante, l'ADN précipite (phénomène de « relarguage ») (pour les mêmes raisons que les protéines). De plus cette
précipitation est facilitée en présence d'éthanol (ou d'isopropanol) car l'ADN y est insoluble.
Ces propriétés sont utilisées dans les protocoles de purification et de fractionnement de l'ADN (cf TP extraction ADN).
*Application: Un procédé classique de purification de l'ADN consiste à traiter une solution aqueuse d'ADN par le phénol qui dénature les
protéines. Le mélange phénol-chloroforme est généralement utilisé car il est plus efficace. Les phases sont séparées par centrifugation:
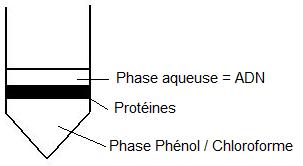
Les traces de phénol (qui pourrait inhiber les enzymes utilisées dans les étapes suivantes) sont éliminées par un nouveau traitement au chloroforme.
Rq: lorsque l'acide nucléique provient directement d'extraits cellulaires, il est généralement traité par des enzymes protéolytiques (protéinase K) afin d'hydrolyser les protéines au préalable.
Viscosité
Les solutions d'ADN ont une grande viscosité en raison de la grande longueur de la double hélice et de sa rigidité; les mesures de viscosité permettent de suivre la dénaturation de l'ADN.
3. L'ARN: Structure, Diffférents Types Et Propriétés
Structure
Les ARN sont des polymères de RiboNucléotides liés par des liaisons phosophodiester 5'-3'. Les bases azotées sont A-U, C-G. Le sucre est le Ribose.
L'ARN est une molécule monocaténaire, c'est-à dire simple brin. Cependant il existe des structures où il y a un repliement en « doubles brins ».
Classification des ARN
La classification des ARN est liée à leurs fonctions. Chaque type d'ARN possède des éléments structuraux propres.
ARN ribosoinaux (ARNr) (80% de l'ARN)
- Structure
- Chez les bactéries:
Les ribosomes ont une constante de sédimentation de 70S. On peut les dissocier en 2 sousunités de 50S et 30S (les constantes de sédimentation ne sont pas additives...). Ainsi:

- Chez les Eucarvotes:
Les ribosomes ont une constante de sédimentation de 80S ≠ 60S + 40 S.

- Localisation des ribosomes
- dans le cytoplasme à l'état libre (synthèse des protéines cytoplasmiques).
- dans le cytoplasme, liés au réticulum endoplasmique (protéines à destination membranaire ou intra-organite).
- dans les mitochondries et les chloroplastes: toutefois, ces ribosomes se rapprochent de ceux des bactéries (cf théorie endosymbiotique...).
Noter que les ARNr sont synthétisés dans le noyau à partir de l'ADN et s'assemblent au niveau des nucléoles avec les protéines, puis passent dans le cytoplasme.
- Fonction des ribosomes
ARN messagers (ARNm) (5% de l'ARN)
- Structure
- Localisation des ARNm
- Fonction des ARNm
ARN de transfert (ARNt) (15% de l'ARN)
- Structure
- petite taille: de 73 à 93 nucléotides.
- structure typique en trèfle, avec de nombreuses régions en structure II (appariement de bases).
- existence d'un anticodon: triplet de nucléotides, complémentaire des codons de l'ARNm
- l'extrémité 3'OH fixe l'acide aminé correspondant au codon de l'ARNm. Elle possède la séquence CCA (constante pour tous les ARNt)
- présence de nombreux nucléotides modifiés (environ 1 sur 10).
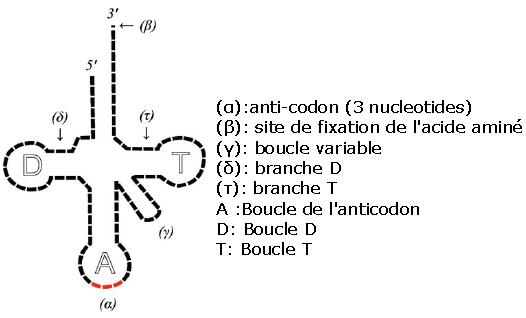
- Localisation et fonction des ARNt
En effet, ils apportent les acides aminés aux ribosomes pour construire les protéines. Ils sont qualifiés d'adaptateurs. Il existe une soixantaine d'ARNt différents (compte tenu de dégénérescence du code génétique, cf plus loin).
ARN chez les Virus
De nombreux virus possèdent un génome à base d'ARN:
- Certains possèdent un ARN bicaténaire, en hélice, analogue à l'ADN. C'est le cas de virus des végétaux.
- les virus à ARN monocaténaire possèdent une ou plusieurs molécules d'ARN (cf le virus HIV qui en a 2).
Propriétés de l'ARN
Ce sont globalement les mêmes que l'ADN.
* Comme l'ADN, il présente un maximum d'absorption à 260 nm, donc on peut le doser également à cette longueur d'onde
* Solubilité:
- Les propriétés de solubilité des ARN sont équivalentes à celles de l'ADN. Il existe cependant une petite différence: les ARN ne précipitent pas
à 0,1 mol.L-1 en NaCl, mais restent solubles. Cela permet de les séparer facilement de l'ADN.
- Les ARN sont précipitables par les cations lourds (exemple: Li+)
* L'ARN est sensible à l'hydrolyse alcaline (cf plus loin) contrairement à l'ADN.
4. Détermination Des Séquences Des Acides Nucléiques
La détermination de la séquence des acides nucléiques est réalisée selon un procédé analogue à celui du séquençage des protéines,
à savoir: hydrolyse chimique ou enzymatique suivie d'une séparation des fragments par chromatographie ou électrophorèse. Des méthodes
modernes existent depuis une vingtaine d'années, que nous verrons également.
La détermination de la séquence de acides nucléiques et bien plus difficile que celle des protéines, car il n'existe que 4 bases dans un acide
nucléique donné (au lieu de 20). Les premières séquences ont été réalisées sur des ARNt, du fait de leur faible taille et de la présence de bases
"anormales" qui servent de point de repère..
Méthodes d'hydrolyse de l'ADN et de l'ARN
Hydrolyse alcaline des ARN
L'hydrolyse alcaline se fait selon un mécanisme impliquant un composé intermédiaire cyclique 2'-3' (via le phosphate). Après rupture des liaisons phosphodiester, on obtient un mélange de nucléosides 2' et 3' monophosphates et l'hydrolyse des ARN est ainsi totale. En revanche, les ADN sont résistants à l'hydrolyse alcaline car ils n'ont pas de -OH sur le C2'.
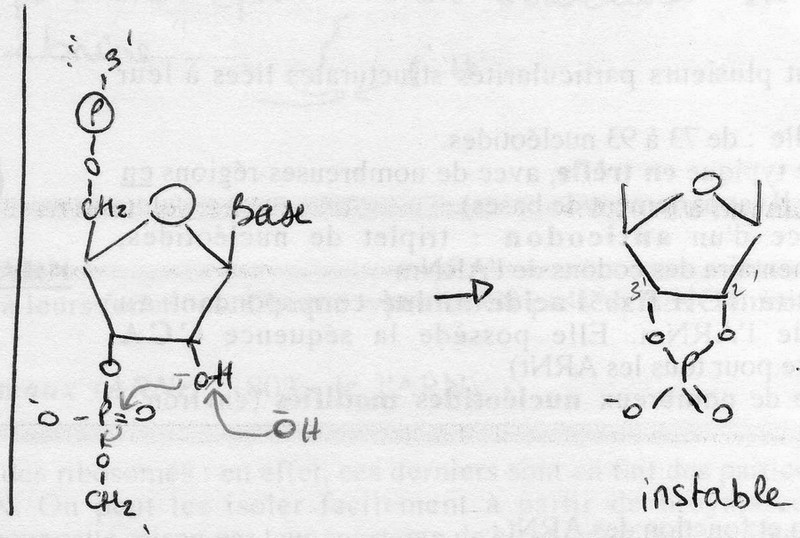
Hydrolyse par les RNases
- RNase pancréatique
- Elle a une certaine spécificité: elle ne coupe que si le nucléotide du côté 3 est pyrimidique. Elle libère donc des oligonucléotides 3'phosphate.

- RNase T1
- RNase U2
Son intérêt est de l'utiliser en complément de la RNase 77. En effet, on fait agir dans un premier temps la RNase Tl, puis, sur les fragments obtenus, on fait agir la U2 qui coupe alors du côté des A.
Hydrolyse par les phosphodiestérases
- Phosphodiestérase de venin de serpent
- Elle libère cette fois des nucléosides 5'P et agit de manière récurrente.
- Elle agit sur l'ADN et sur l'ARN simple brin.
- Phosphodiestérase de rate
- Elle hydrolyse à partir du côté 5', si celui-ci est non phosphorylé.
- Elle libère des nucléosides 3'P et agit de manière récurrente.
Hydrolyse par la phosphatase alcaline
Il s'agit d'une enzyme qui détache les groupements phosphates situés aux extrémités d'un polynucléotide. On qualifie ce type d'enzyme, pour cette raison, de phosphomonoestérase (et non plus de phosphodiestérase).
Action des DNases
Il s'agit d'endonucléases. Les premières DNAses connues était moins spécifiques que les RNAses. On peut citer:
- la DNase I (= DNAse pancréatique): elle engendre des nucléosides 5'P.
- la DNase II (= DNAse acide): elle engendre des nucléosides 3'P.
Il existe chez les bactéries des endonucléases beaucoup plus spécifiques, qui digèrent l'ADN au niveau de séquences très particulières (double
brin). Ce sont les endonucléases de restriction. Elles servent aux bactéries à digérer tout ADN étranger qui s'introduirait dans la cellule, comme
celui des bactériophages (l'ADN homologue est protégé par méthylation d'une bases sur chaque brin au niveau du site de coupure). Elles coupent
l'ADN bicaténaire au niveau de courtes séquences (4 à 6 nucléotides),Je plus souvent symétriques (= palindromes) et présentes en très petit nombre
dans les molécules d'ADN.
Exemple:

Application:
La coupure par une endonucléase du type EcoR I ou BamHI produit des fragments possédant des extrémités cohésives = des extrémités monocaténaires ayant des séquences complémentaires: ceci permet de souder spécifiquement 2 fragments d'ADN ayant des origines différentes, mais ayant été hydrolyses par la même endonucléase de restriction. Cette propriété est utilisée lors d'expérience de recombinaison in vitro, en particulier pour introduire des séquences d'ADN d'origine diverse dans des phages ou des plasmides (cf cours génie génétique).

Détermination de la séquence des acides ribonucléiques
Le séquençage de l'ARN est utilisé pour déterminer la séquence des ARNr, ARNt, ou encore l'ARN génomique de certains virus (= à ARN). Pour cela, plusieurs techniques sont utilisables.
Hydrolyse enzymatique suivie de séparation des fragments
A l'aide des différentes techniques vues au §4.1, on réalise l'hydrolyse partielle ou totale puis on sépare les fragments obtenus:
- par chromatographie d'exclusion en colonne: méthode lourde car elle nécessite une grande quantité de matériel, mais permet par la suite la
caractérisation des nucléotides, en particulier les nucléotides rares.
- par électrophorèse sur gel d'agarose ou de polyacrylamide: cette technique requiert le marquage radioactif des ARN au 32P, pour permettre la
visualisation des fragments d'ARN (par application d'un film d'autoradiographie sur l'électrophorégramme).
Rq: marquage radioactif de l'ARN:
- in vivo, en cultivant les cellules sur un milieu contenant du 32P,
- in vitro, après coupure par les enzymes,
- en remplaçant le phosphate en 5' par du phosphate contenant du 32P,
- ou en ajoutant en 3'-OH un phosphate contenant du 32P.
Cas d'ARN courts (<70 nucléotides)
Seule l'extrémité 5' de l'ARN est marquée au 32P (par une polynucléotide kinase et de l'ATP32Pγ).
On soumet ensuite différents aliquotes à une digestion enzymatique par différentes enzymes spécifiques (cf §4.1) dans des conditions, où,
statistiquement il n'y aura qu'une coupure par chaîne.
Les fragments sont ensuite fractionnés par électrophorèse sur gel de polyacrylamide: seuls les fragments marqués au 32P seront visualisables par
autoradiographie.
Parallèlement une hydrolyse alcaline plus ou moins partielle permet de générer des fragments de toutes les tailles possibles = repères.
Détermination de la séquence des acides désoxyribonucléiques
Depuis 20 ans, des méthodes ont été mises au point pour déterminer la séquence de l'ADN.
L'ADN à séquencer étant parfois de taille importante, on procède en plusieurs étapes:
- hydrolyse de l'ADN par les endonucléases de restriction
- séparation des fragments et séquençage de ceux-ci. Pour ce séquençage, 2 méthodes existent.
La méthode de Maxam et Gilbert
Le principe est semblable à celui présenté pour les ARN, sauf que l'ADN est hydrolyse de manière chimique et non enzymatique.
1- Le fragment d'ADN est marqué au 32P à une extrémité, et divisé en 4 aliquots.
2- Chacun d'eux est soumis à une hydrolyse chimique différente, dans des conditions telles qu'il n'y ait qu'une coupure (ou un faible nombre de
coupures) par chaîne.
- un traitement au diméthylsulfate, qui méthyle surtout la guanine en N7; sous l'effet de la chaleur, la guanine est détachée et la chaîne
polynucléotidique est rompue à ce niveau: on obtient des fragments se terminant par une guanine.
- un traitement au diméthylsulfate en milieu acide, qui méthyle la guanine en N7 et l'adénine en N3: on obtient des fragments se terminant là où
dans la chaîne, il y avait une guanine et une adénine. Par comparaison avec la réaction précédente, on en déduit la position des adénines.
- un traitement par l'hydrazine en milieu NaCl 1 mol.L-1 permet de déterminer les fragments se terminant par C
- un traitement par l'hydrazine sans NaCl permet de couper au niveau des C et des T. Par comparaison avec la réaction précédente, on en déduit la
position des thymidines.
3- Les fragments engendrés par ces 4 réactions sont séparés en parallèle par électrophorèse sur gel de polyacrylamide en fonction de leur taille.
Le fragment le plus court se retrouve au bas du gel, le plus long en haut.
Deux fragments successifs ont une taille qui ne diffère que d'un seul nucléotide.
4- La révélation se fait par autoradiographie. On lit ainsi, de bas en haut, la séquence de l'ADN sur une autoradiographie.
Actuellement, on sépare des fragments allant de 1 à 300 nucléotides (gels de 40 cm de long). Pour établir la séquence de fragments d'ADN plus longs,
on répète l'opération sur des fragments de préférence légèrement chevauchants obtenus par différentes enzymes de restriction.
La méthode de Sanger, dite des « didéoxynucléotides » (Nobel en 1976)
Cette méthode est pratiquement utilisée à l'heure actuelle à la place de la précédente.
- L'ADN à séquencer est clone (c-à-d inséré) sous forme simple brin dans un vecteur particulier, le phage M13.
- On utilise ce fragment pour réaliser, au moyen de l'ADN polymérase I, le brin complémentaire (on fait en fait, grâce à une amorce,
une réplication in vitro ). La réplication nécessite des nucléotides tnphosphates dNTP. L'un d'eux est marqué par du 32P sur le P.
- On réalise 4 réactions de polymérisation indépendantes, en introduisant dans chaque cas un type de didéoxynucléotide = ne possédant d'-OH ni en
2', ni en 3'. Lorsqu'un tel nucléotide est incorporé, il y a donc arrêt de la synthèse. Le rapport ddNTP/dNTP (pour 1 N donné) est tel que qu'on
arrive à avoir une incorporation de ddNTP au hasard et donc des fragments de tailles différentes ayant tous le ddNTP en 3'.
- On obtient ainsi une série de fragments d'ADN ne différant que d'un seul nucléotide et se terminant par un didéoxynucléotide. On peut alors,
après électrophorèse et autoradiographie, lire de bas en haut la séquence du brin néosynthétisé (= complémentaire du brin ayant servi de matrice),
et donc en déduire la séquence du brin d'ADN de départ.
Annexe
Version Pdf
Première partie, Version imprimable en pdfSeconde partie, Version imprimable en pdf