Biologie Moléculaire et Cellulaire
Introduction aux outils du génie génétique
Les enzymes du génie génétique
Au cours du clonage d'un gène, il est nécessaire d'obtenir de l'ADN purifié et de construire une nouvelle
molécule d'ADN recombinée, c'est à dire introduire une petite molécule d'ADN dans un vecteur. Pour cela, il est
nécessaire de couper les molécules d'ADN en des sites spécifiques : l'ADN à cloner et le vecteur, pour les
fusionner de façon contrôlée.
D'autres manipulations peuvent être réalisées : raccourcissement, allongement, copies en de nouvelles molécules
ADN ou ARN, modifiées ou non...
Ces différentes manipulations sont effectuées avec des enzymes spécifiques.
1. Les nucléases
Définition : les nucléases dégradent les molécules d'ADN en rompant les liaisons phosphodiesters liant un
nucléotide au suivant (voir cours de biochimie pour liaison phosphodiester).
Il existe 2 types de nucléases.
Exonucléases
Ces enzymes éliminent des nucléotides un à un à partir d'une extrémité de l'ADN. Il en existe différents types, par exemple la Bal31 (obtenue de cultures d'Aliéromonas espejana) éliminant des nucléotides à partir des 2 extrémités des 2 brins, l'exonucléase 3 (obtenue à partir de cultures d'E. coli) catalysant l'hydrolyse séquentielle des nucléotides d'un ADN à partir d'une extrémité 3' libre.
Endonucléases
A clivages non spécifiques:
Ces enzymes sont capables de rompre des liaisons phosphodiesters internes.
La DNAse I extraite du pancréas, coupe préférentiellement après une base pyrimidique en utilisant une extrémité
3'OH et une 5' phosphate libre aussi bien les ADN simple brin que double brins.
La nucléase SI, extraite de culture d'Aspergillus oryzae dégrade seulement les acides nucléiques monocaténaires.
A clivages spécifiques: enzymes de restriction:
Elles coupent de manière définie et reproductible l'ADN bicaténaire. Ce sont les enzymes permettant l'ouverture
spécifique du vecteur et le découpage défini de l'ADN à cloner. Ce sont des enzymes produites par de très
nombreuses bactéries au moment des infections lysogéniques (voir cours sur la lysogénie).
L'analyse de leurs coupures de l'ADN montre qu'elles se font en des sites spécifiques. Plus de 1200 différentes
enzymes de restriction ont été caractérisées et elles sont classés en 3 types :
type I: l'enzyme reconnaît sa séquence puis se déplace sur l'ADN et s'arrête de manière aléatoire 1000 à
5000 paires plus loin et libère quelques dizaines de nucléotides.
type II: une fois la séquence reconnue, l'enzyme coupe l'ADN au niveau de cette séquence (les plus courante
en biologie moléculaire).
type III: après reconnaissance de la séquence spécifique, ces enzymes découpent l'ADN une
vingtaine de nucléotides plus loin.
La longueur des séquences reconnue est comprise entre 4 et 8 bases. Elle est identique sur les 2 brins. Par
exemple ECO RI reconnaît la séquence:
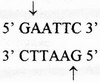
Les enzymes de restriction de type II provoquent 2 types de coupure:
- coupures à bouts francs. Les enzymes coupent exactement au même niveau les 2 brins d'ADN : exemple Puu II qui coupe:
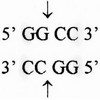
- coupures à bouts cohésifs ou protusifs. Dans ce cas, les coupures sont décalées l'une par rapport à l'autre. C'est le cas d'ECO R1 précédemment décrit. Les parties simple brin complémentaire peuvent s'apparier. Ainsi, grâce à ce type d'enzymes, 2 ADN d'origine différente coupées par une même enzyme de restriction produisant des extrémités cohésives peuvent être mis bout à bout puis ligaturés. C'est une propriétés très utilisée dans les recombinaisons génétiques in vitro.
2. Les polymérases et enzymes apparentées
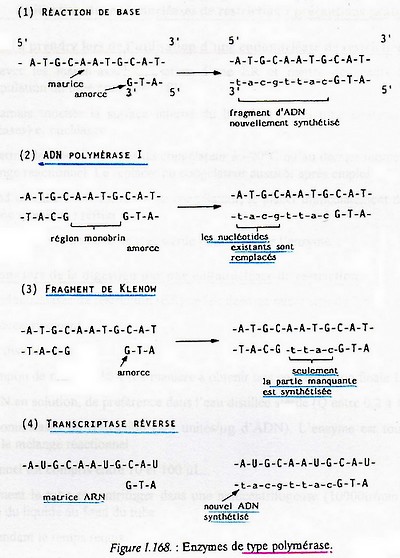
Les polymérases d'acides nucléiques sont des enzymes qui synthétisent un nouveau brin d'ADN complémentaire à une matrice d'ADN ou ARN. La plupart des polymérases ne peuvent fonctionner que si la matrice d'ADN ou d'ARN possède une région double brin qui agit comme amorce pour l'initiation de la polymérisation. Trois types de polymérases sont couramment utilisées en géni génétique :
ADN polymérase I
Extraite d'Eschérichia coli, elle joue un rôle majeur dans la réparation de l'ADN. L'enzyme se fixe à une région monobrin et synthétise totalement le brin complémentaire, dégradant au fur et à mesure la partie existante du brin (activité nucléasique). L'activité polymérasique s'effectue dans le sens 5' vers 3' à partir d'une amorce 3'OH. L'ADN synthétisée est strictement complémentaire de la matrice.
Fragment de Klenow
Le fragment de Klenow ne possède pas d'activité nucléasique et peut synthétiser un brin complémentaire d'ADN à
partir d'une matrice monobrin.
La T4 polymérase possède les mêmes propriétés.
Transcriptase réverse
Codée par les gènes pol des rétrovirus, cette enzyme transcrit TARN en ADN complémentaire (cADN). Comme toutes les polymérases, elle travaille dans le sens 5' vers 3'. Elle peut aussi utiliser l'ADN comme matrice.
3. Enzymes modifiant l'ADN
De nombreuses enzymes modifient l'ADN par addition ou suppression de groupes chimiques spécifiques. Les
principales sont:
La phosphatase alcaline: elle retire le phosphate en 5' sur l'ADN, l’ARN et les nucléotides libres.
L'élimination des phosphates en 5' empêche toute action des ligases. Un vecteur ouvert ainsi traité ne pourra pas
se refermer sur lui même et cette fermeture redeviendra possible par intégration d'un ADN étranger.
La T4 polynucléotide kinase: elle transfère le phosphate d'un ATP sur le phosphate en 5' d'un
polynucléotide. Ce marquage en 5' s'effectue en vue de déterminer la séquence d'un ADN.
Les topopisomérases: l'état physiologique de l'ADN est la forme superenroulée. Les topoisomérases sont
capables de changer cette conformation. Ces enzymes sont surtout importantes pour l'étude de la réplication de
l'ADN.
4. Ligases
Dans la cellule, l'ADN ligase répare les discontinuités qui peuvent apparaître dans un ADN double brins, notamment lors de la réplication Ce type d'enzyme permet de relier les 2 fragments d'ADN double brins C'est une enzyme capitale puisqu'elle permet la construction de molécules d'ADN recombinées.
ADN ligase
L'enzyme n'agit que si les 2 ADN sont associés par des extrémités cohésives (voir enzymes de type II). Cette ligase assure la formation des liaisons phosphodiesters entre une extrémité 3'OH et une extrémité 5' phosphate.
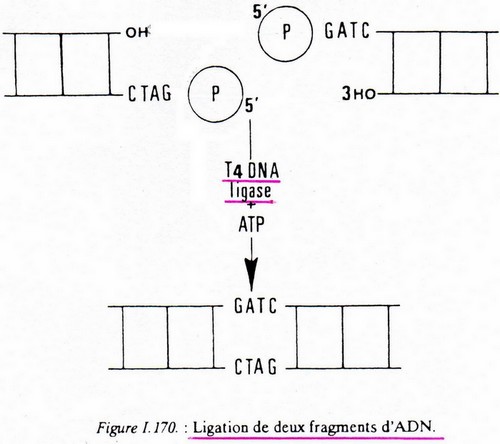
T4 ADN ligase
Elle est capable d'effectuer des ligations entre 2 ADN à bouts francs.
Utilisation des endonucléases de restriction : précautions pratiques
Précaution à prendre lors de l'utilisation d'une endonucléase de restriction
- Se laver les mains avant utilisation d'une ER et mettre des gants à usage unique avant la manipulation du tube
contenant l'ER.
- Ne jamais toucher la surface interne du bouchon et du tube contenant l'ER (la peau possède protéases) et
nucléases.
- Ne retirer le tube d'enzymes du congélateur à -20°C qu'au dernier moment, juste avant addition au mélange
réactionnel. Le replacer au congélateur aussitôt après emploi.
- Quand un tube d’ER est retiré du congélateur, le placer immédiatement dans la glace pilée ou dans un bloc
métallique réfrigéré.
- Utiliser toujours un cône neuf et stérile pour prélever l'enzyme.
Précautions lors de la digestion par une endonucléase de restriction
L’utilisation des endonucléases de restriction (ER) se fait dans un microtube de 1,5mL maintenu dans la glace.
II faut introduire successivement:
- l'eau distillée stérile
- le tampon de réaction 10X (de manière à obtenir une concentration finale 1X)
- l'ADN en solution, de préférence dans l'eau distillée stérile (Q entre 0,2 à 10 μg)
- l’endonucléase de restriction (2/3 unités/μg d'ADN). L'enzyme est toujours rajoutée en dernier dans le mélange
réactionnel.
Le volume réactionnel est compris entre 10 et 100 μL.
Puis agiter doucement le tube et centrifuger dans une minicentrifugeuse (10 000tr/min) quelques secondes pour
collecter la totalité du liquide au fond du tube.
Incuber à 37 °C pendant le temps requis.
Stopper la réaction enzymatique soit par addition d'EDTA à 0,5 mol.L-1 (pH 7,5) à la concentration finale de 10
nmol.L-1, soit par addition de solution de charge si l'ADN est aussitôt analysé dans un gel.
Mélanger en vortexant rapidement et centrifuger à 12000 tr/min pour collecter la totalité du liquide et éliminer les
bulles.
Annexes
Schémas

Version Pdf
Version imprimable en pdfAutres Documents Pdf - Introductions aux Techniques de Travaux Pratiques
Electrophorèse sur gel d'AgaroseCulture de cellules animales